CÁC YẾU TỐ CÂN NHẮC LỰA CHỌN ĐIỀU TRỊ TOÀN THÂN BƯỚC 2 UNG THƯ BIỂU MÔ TẾ BÀO GAN KHÔNG THỂ PHẪU THUẬT ĐƯỢC: CA LÂM SÀNG TẠI BỆNH VIỆN K
BSCKII. Nguyễn Thị Hương
Phó giám đốc TT Chăm sóc giảm nhẹ, Bệnh viện K2
1. Tổng quan
Ung thư biểu mô tế bào gan (UTBMTBG), hay còn được biết đến là Hepatocellular carcinoma (HCC), là một loại ung thư xuất phát từ tế bào gan và thuộc nhóm bệnh ung thư gan (UTG), bao gồm cả ung thư đường mật trong gan và sarcoma. Theo thống kê của GLOBOCAN 2020 trên toàn cầu, trong các loại ung thư phổ biến, UTG đứng ở vị trí thứ 7 về tỉ lệ mắc mới và thứ 3 về tỉ lệ gây tử vong [1]. Ở Việt Nam, UTG chiếm vị trí hàng đầu về cả tỉ lệ mắc mới và tỉ lệ tử vong, và xuất hiện dấu hiệu tăng lên theo thời gian [2]. Trong số các trường hợp UTG, UTBMTBG chiếm đến 85%, với nguyên nhân chủ yếu là viêm gan virus B-C và xơ gan do rượu. Việt Nam được xác định là một trong những quốc gia có tỉ lệ mắc bệnh UTBMTBG cao nhất trên thế giới, và các nghiên cứu dịch tễ cho thấy rằng viêm gan virus B là nguyên nhân phổ biến nhất [3].
Kéo dài thời gian sống còn luôn là mục tiêu then chốt trong điều trị Ung thư biểu mô tế bào gan quá chỉ định phẫu thuật (uHCC). Cũng giống như điều trị Ung thư khác, bệnh nhân uHCC càng tiếp cận được với nhiều bước điều trị thì càng tăng cơ hội kéo dài thời gian sống còn .
Hiện tại, ở Việt Nam, các thuốc điều trị toàn thân được phê duyệt bao gồm: điều trị bước 1 (sorafenib, lenvatinib, atezolizumab phối hợp bevacizumab), điều trị bước 2 (regorafenib, pembrolizumab) [4]. Với việc xuất hiện thêm nhiều lựa chọn trong điều trị, việc lựa chọn và tối ưu điều trị trở nên quan trọng và cần cá thể hóa điều trị.
Các yếu tố cân nhắc trong lựa chọn điều trị bước 2 trong UTBMTBG:
- Tính sẵn có của thuốc tại Việt Nam
- Khuyến cáo điều trị: BCLC 2022, NCCN 2023, ESMO…..
- Hiệu quả điều trị dựa trên dữ liệu thử nghiệm lâm sàng, và dữ liệu đời thực
- Hồ sơ an toàn: tác dụng ngoại ý và các biện pháp phòng ngừa & xử lý tác dụng ngoại ý
- Kế hoạch điều trị: cân nhắc lựa chọn điều trị bước 2 dựa trên lựa chọn và đáp ứng điều trị bước 1 trước đó
- Chi phí điều trị: bảo hiểm y tế và chương trình hỗ trợ thuốc miễn phí một phần
2. Báo cáo ca lâm sàng
- Họ tên: (tên viết tắt): NGUYỄN VĂN V
- Tuổi/Giới: 1959
- Ngày vào viện: 23/12/2021
- Lý do: BV Việt Đức chuyển tới sau mổ cắt gan

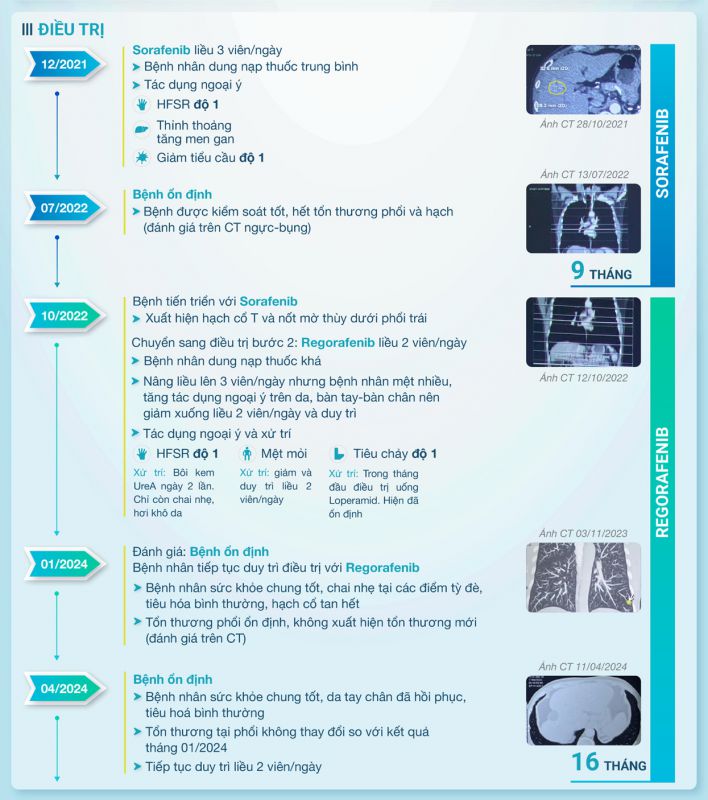
3. Bàn luận
3.1. Lựa chọn điều trị bước 2 sau khi tiến triển với sorafenib bước 1:
Hiện tại, ở Việt Nam có 2 thuốc có chỉ định phê duyệt trong điều trị bước 2 sau tiến triển với sorafenib bước 1 là regorafenib và pembrolizumab. Hiện chưa có nghiên cứu đối đầu giữa 2 thuốc này. Do đó, cân nhắc lựa chọn điều trị bước 2 cho trường hợp bệnh nhân này, chúng tôi căn cứ vào 1 số yếu tố sau:
- Khuyến cáo điều trị
- Hiệu quả điều trị dựa trên kết quả thử nghiệm lâm sàng và dữ liệu đời thực
- Tính an toàn
- Chi phí điều trị
Regorafenib
Thử nghiệm RESORCE là một thử nghiệm ngẫu nhiên, mù đôi, đối chứng giả dược pha III chứng minh hiệu quả của Regorafenib ở những bệnh nhân đã tiến triển sau điều trị bằng Sorafenib. Kết quả cho thấy Regorafenib cải thiện thời gain sống còn mOS 10.6 tháng, mPFS là 3,1 tháng, và tỷ lệ kiểm soát bệnh DCR là 65%, so với tương ứng ở nhóm giả dược mOS 7,8 tháng; mPFS 1,5 tháng, và DCR là 36%.
Theo khuyến cáo NCCN, mức độ bằng chứng khuyến cáo điều trị regorafenib bước 2 là IA (mức độ mạnh). Ngoài ra, regorafenib điều trị bước 2 được nhắc tới trong các khuyến cáo của Bộ Y tế Việt Nam, BCLC, ESMO, ….
Trong phân tích RESORCE mở rộng, chuỗi điều trị sorafenib – regorafenib cho thấy trung vị kéo dài thời gian sống còn là 26 tháng. Đây được coi là chuỗi điều trị duy nhất tại thời điểm hiện tại có dữ liệu thử nghiệm lâm sàng RCT.
.jpg) Khuyến cáo lựa chọn điều trị HCC theo Barcelona Clinic Liver Cancer 2022
Khuyến cáo lựa chọn điều trị HCC theo Barcelona Clinic Liver Cancer 2022
Pembrolizumab
Trong nghiên cứu pha II KEYNOTE-224, pembrolizumab cho thấy có lợi ích về OS và ORR lần lượt là 12,9 tháng và 17%. Tuy nhiên, thử nghiệm pha III KEYNOTE-240 so sánh pembrolizumab điều trị bước 2 với chăm sóc nâng đỡ ở những bệnh nhân HCC đã thất bại với Sorafenib bước 1 là một thử nghiệm âm tính.
Theo khuyến cáo NCCN, mức độ bằng chứng khuyến cáo điều trị pembrolizumab bước 2 là IIB
 .
.
3.2. Tối ưu hiệu quả điều trị bước 2 với regorafenib
Không phải tất cả bệnh nhân tiến triển sau bước 1 đều là ứng cử viên cho điều trị bước 2 với Regorafenib. Trong thực hành lâm sàng, chỉ có khoảng 30% bệnh nhân đủ điều kiện điều trị bằng Regorafenib bước 2 vì chức năng gan và tình trạng hoạt động cơ thể của bệnh nhân bị suy giảm đáng kể sau điều trị bước 1.
Do đó, để tối ưu điều trị bước 2 với regorafenib, việc lựa chọn bệnh nhân phù hợp là một yếu tố quan trọng.
Theo khuyến cáo NCCN, chiến lược liều tăng dần 80mg – 120mg – 160 mg với regorafenib nên được cân nhắc để quản lý tác dụng ngoại ý, tăng tuân thủ điều trị của bệnh nhân mà không ảnh hưởng giảm hiệu quả điều trị so với điều trị liều khuyến cáo 160mg ngay từ đầu. Do đó, với trường hợp bệnh nhân này thời điểm ban đầu sức khoẻ sau mổ không được tốt, men gan cao, tiểu cầu giảm, xơ gan. Vì vậy, bệnh nhân dùng liều khởi đầu 80 mg regorafenib bước 2 ban đầu. Mức liều này giúp giảm tác dụng ngoại ý (HFSR, hệ tiêu hóa). Ngoài ra, Bệnh nhân có chất lượng sống ổn định nhờ vào phối hợp thuốc hỗ trợ. Trong quá trình điều trị, bệnh nhân được theo dõi và đánh giá lâm sàng, cận lâm sàng đúng định kỳ 3 tháng/lần.
4. Kết luận
Thông qua ca lâm sàng bệnh nhân ung thư biểu mô tế bào gan được điều trị bằng chuỗi Sorafenib-Regorafenib tại khoa Chăm sóc giảm nhẹ, bệnh viện K2 cho thấy hiệu quả điều trị chuỗi và tính an toàn hoàn toàn đồng nhất với dữ liệu lâm sàng đã được báo cáo, bao gồm:
- Thời gian điều trị bước 1 với Sorafenib là 9,0 tháng
- Thời gian điều trị bước 2 với Regorafenib tính đến hiện tại là 16,0 tháng và còn tiếp tục tăng.
- Tác dụng ngoại ý (HFSR, mệt mỏi, tiêu chảy) thường xuất hiện sớm, độ 1 và có thể quản lý được bằng cách hiệu chỉnh liều điều trị phù hợp và các biện pháp hỗ trợ như kem bôi da, thuốc tiêu chaỷ. Kết hợp chăm sóc giảm nhẹ và điều trị bổ trợ góp phần nâng cao chất lượng cuộc sống và giảm nhẹ triệu chứng khó chịu của tác dụng ngoại ý.
Tài liệu tham khảo
- Hyuna Sung PhD, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA: A Cancer Journal for Clinicians. 2021; 71(3): 209-249. doi: 10.3322/caac.21660.
- Linh Ha, et al. Proportion and number of cancer cases and deaths attributable to behavioral risk factors in Vietnam. International Journal of Cancer. 2023; 153(3): 524-538. doi: 10.1002/ijc.34549.
- Josep M. Llovet, et al. Hepatocellular carcinoma. Nature Reviews Disease Primers. 2021; 7(6). doi: 10.1038/s41572-020-00240-3.
- Quyết định số 3129/QĐ-BYT ngày 17 tháng 07 năm 2020 về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị ung thư biểu mô tế bào gan”
- Finn R et al. J Hepatol. 2018;69:353-358.
Bài trình bày do Công ty Astellas tài trợ và Hội Gan mật Việt Nam đồng hành.

- Kỷ yếu hội thảo thường niên kỷ niệm ngày viêm gan thế giới với chủ đề Chung tay đánh gục Virut Viêm gan, cùng đẩy lùi Xơ gan và Ung thư gan
- Ứng dụng kỹ thuật MRI xung mDIXON quant kết hợp AI trên phần mềm Liver Health để định lượng gan nhiễm mỡ và quá tải sắt 3D tự động theo từng phân thuỳ và toàn bộ gan
- Chiến lược điều trị chuỗi trong Ung thư biểu mô tế bào Gan: Dữ liệu đời thực và ca lâm sàng tại Bệnh viện Ung bướu Hà Nội.
- Kỷ nguyên mới trong điều trị ung thư biểu mô tế báo gan tiến triển: Lựa chọn điều trị bước 2 và thời điểm thích hợp để chuyển bước điều trị
- TIẾP CẬN ĐIỀU TRỊ NHIỀU BƯỚC VỚI LIỆU PHÁP TOÀN THÂN NHẰM KÉO DÀI SỐNG CÒN TRONG UNG THƯ BIỂU MÔ TẾ BÀO GAN: BÀN LUẬN CA LÂM SÀNG
- ĐIỀU TRỊ ĐA MÔ THỨC CHO UNG THƯ BIỂU MÔ TẾ BÀO GAN QUÁ CHỈ ĐỊNH PHẪU THUẬT: ĐÁNH GIÁ QUA CA LÂM SÀNG TACE PHỐI HỢP ĐIỀU TRỊ TOÀN THÂN
- HIỆU QUẢ CỦA ĐIỀU TRỊ ĐA MÔ THỨC CHO UNG THƯ BIỂU MÔ TẾ BÀO GAN QUÁ CHỈ ĐỊNH PHẪU THUẬT: ĐÁNH GIÁ QUA CA LÂM SÀNG ĐƠN LẺ
- HIỆU QUẢ ĐIỀU TRỊ XƠ GAN DO HBV BẰNG CÁC THUỐC NAs
- TỐI ƯU HÓA ĐIỀU TRỊ VIÊM GAN VI RÚT C MẠN TÍNH
- CẬP NHẬT TIẾN BỘ MỚI TRONG CHẨN ĐOÁN & ĐIỀU TRỊ BỆNH GAN NHIỄM MỠ KHÔNG DO RƯỢU
- Vietnam Association of the Study of Liver Disease Hanoi City, Vietnam
- HBV cccDNA: CON ĐƯỜNG HÌNH THÀNH, VAI TRÒ VÀ NGUYÊN LÝ ĐỊNH LƯỢNG
- Virus viêm gan Delta: Nguy cơ gây bệnh gan tiến triển nhưng chưa được quan tâm
- HBV cccDNA: sự dai dẳng của nó trong nhân tế bào gan bị nhiễm là thách thức chủ yếu đối với sự điều trị khỏi chức năng nhiễm HBV mạn
- GIÁ TRỊ CỦA CÁC XÉT NGHIỆM TRONG QUẢN LÝ BỆNH VIÊM GAN VI RÚT B MẠN
- Cập nhật các dấu ấn sinh học phân tử trong tầm soát phát hiện sớm ung thư gan ở bệnh nhân nhiễm HBV mạn tính
- CHIẾN LƯỢC TIẾP CẬN MỚI TRONG ĐIỀU TRỊ BỆNH NHÂN VIÊM GAN B
- Điều trị toàn thân cho bệnh nhân UTBMTBG quá chỉ định phẫu thuật giai đoạn trung gian
- CẬP NHẬT VỀ CÁC KỸ THUẬT ĐO ĐÀN HỒI GAN
- Tình hình bệnh Viêm gan vi rút và Đáp ứng ở Việt Nam
- Implementing living donors pediatric liver transplantation program: children hospital 2 experience
- viêm tụy mạn sỏi tụy trên bệnh nhân không uống rượu
- KẾT QUẢ SỐNG THÊM LÂU DÀI SAU TẮC MẠCH XẠ TRỊ Ở BỆNH NHÂN UNG THƯ BIỂU MÔ TẾ BÀO GAN KHÔNG CÒN CHỈ ĐỊNH PHẪU THUẬT
- Viêm gan chưa rõ nguyên nhân ở trẻ em
- Nhiễm Viêm gan B: Các tiến bộ và quần thể bệnh nhân đặc biệt
Tin cùng loại

 VN
VN
 EN
EN