Kết quả sống thêm lâu dài của bệnh nhân ung thư biểu mô tế bào gan được điều trị bằng phương pháp tắc mạch hóa dầu và tắc mạch hóa chất sử dụng hạt vi cầu DC-Beads
Mục tiêu: Đánh giá kết quả sống thêm lâu dài của các bệnh nhân ung thư biểu mô tế bào gan (UTBMTBG) được điều trị bằng hóa tắc mạch hóa dầu (TACE) và tắc mạch hóa chất sử dụng hạt vi cầu DC Beads (DEB-TACE). Đánh giá một số yếu tố liên quan đến kết quả điều trị giữa 2 nhóm
TÓM TẮT:
Mục tiêu: Đánh giá kết quả sống thêm lâu dài của các bệnh nhân ung thư biểu mô tế bào gan (UTBMTBG) được điều trị bằng hóa tắc mạch hóa dầu (TACE) và tắc mạch hóa chất sử dụng hạt vi cầu DC Beads (DEB-TACE). Đánh giá một số yếu tố liên quan đến kết quả điều trị giữa 2 nhóm
Đối tượng và phương pháp: 280 bệnh nhân UTBMTBG được điều trị bằng phương pháp TACE và DEB-TACE tại Bệnh viện TWQĐ 108 và Bệnh viện 103, từ 05/2014 đến 12/2017. Đánh giá sống thêm từ ngày can thiệp lần đầu tiên, phân tích theo đường cong Kaplan Meier. Sử dụng test log-rank để đánh giá sự khác biệt về thời gian sống thêm trung bình và tỉ lệ sống thêm tại các thời điểm 1 năm, 2 năm và 3 năm theo các phân nhóm theo yếu tố tiên lượng.
Kết quả: Tỉ lệ sống thêm tích lũy tại các thời điểm 1, 2 và 3 năm lần lượt nhóm TACE là: 52,1%; 25,0%; 13,9% và nhóm DEB-TACE là 65,3%; 42,6%; 24,1%. Thời gian sống thêm trung bình của nhóm TACE là 17,1 ± 1,3 tháng, nhóm DEB-TACE là 21,6 ± 1,3 tháng (χ2= 7,1, p= 0,008). Thời gian sống thêm không tiến triển bệnh nhóm TACE là 12,7 ± 1,3 tháng, nhóm DEB-TACE là 17,7 ± 1,4 tháng, (χ2= 11,11, p= 0,001). Nguy cơ tử vong của nhóm TACE tăng cao hơn so nhóm DEB-TACE (p < 0,05) liên quan đến nồng độ AFP huyết (>20 ng/ml) (gấp 1,56 lần); biệt hóa tế bào mức độ kém (gấp 1,37 lần), Okuda I (gấp 2,34 lần), đáp ứng khối u sau điều trị (theo mRECIST) (gấp 1,54 lần).
Kết luận: Kỹ thuật DEB-TACE có hiệu quả điều trị tốt hơn so với nhóm điều trị đơn thuần bằng TACE.
Từ khóa: Ung thư biểu mô tế bào gan, tắc mạch hóa dầu, tắc mạch hóa chất sử dụng hạt vi cầu, sống thêm, yếu tố tiên lượng.
I. ĐẶT VẤN ĐỀ
Ung thư biểu mô tế bào gan (UTBMTBG) là loại ung thư thường gặp, chiếm khoảng 95% các khối u gan ác tính. Trên thế giới, UTBMTBG đứng hàng thứ 6 (tại Việt Nam đứng thứ 5) các loại ung thư ác tính và đứng hàng thứ 3 trong các nguyên nhân gây tử vong do ung thư [1], [2]. Tiên lượng xấu với tỉ lệ sống 5 năm 5% [3]. Cho đến nay, trên thế giới có rất nhiều phương pháp điều trị ung thư gan từ phẫu thuật đến điều trị tạm thời. Tuty nhiên, phẫu thuật hoặc ghép gan vẫn là phương pháp lựa chọn hàng đầu, nhằm mục đích điều trị triệt để ung thư gan.
Năm 2002, hóa tắc mạch qua đường động mạch gan đã được chấp nhận rộng rãi như một phương pháp điều trị tạm thời cơ bản cho bệnh nhân UTBMTBG không còn chỉ định phẫu thuật. Phương pháp tắc mạch hóa dầu (TACE) được định nghĩa là tiêm thuốc chống ung thư vào động mạch gan có hoặc không có Lipiodol, tiếp sau là gây tắc mạch nuôi khối u. Phương pháp tắc mạch sử dụng hạt vi cầu tải hóa chất (DEB-TACE) được phát triển trên cơ sở kỹ thuật hóa tắc mạch truyền thống, với việc sử dụng các hạt vi cầu với hai vai trò vật liệu gây tắc mạch và chất mang hóa chất giải phóng hóa chất một cách bền vững cho phép duy trì nồng độ hóa chất cao và lâu dài hơn trong khối u và giảm nồng độ thuốc ở vòng tuần hoàn chung. Đề tài nghiên cứu nhằm mục tiêu sau:
- Đánh giá hiệu quả sống thêm lâu dài của bệnh nhân UTBMTBG điều trị bằng tắc mạch hóa dầu và tắc mạch hóa chất sử dụng hạt vi cầu.
- Tìm hiểu một số yếu tố tiên lượng đến kết quả sống thêm lâu dài sau điều trị giữa 2 nhóm
II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP.
2.1. Đối tượng: gồm 280 bệnh nhân UTBMTBG, chia thành 2 nhóm: Nhóm điều trị bằng phương pháp tắc mạch hóa dầu (TACE, n = 121) và tắc mạch chất sử dụng hạt vi cầu tải hóa chất (DEB-TACE, n = 159) tại Bệnh viện 103 và Bệnh viện TƯQĐ 108, từ 5/2014 đến 12/2017.
2.1.1. Tiêu chuẩn lựa chọn:
* Là những BN UTBMTBG dựa vào hướng dẫn đồng thuận Quốc tế - Hội Gan mật châu Âu (EASL) năm 2012, Hiệp hội nghiên cứu về bệnh gan của Mỹ (AASLD) năm 2010 hoặc Hướng dẫn chẩn đoán của Bộ Y tế Việt Nam năm 2012:
- Có bằng chứng giải phẫu bệnh.
- Hình ảnh điển hình trên chụp CLVT có tiêm thuốc cản quang hoặc CHT có thuốc cản từ + AFP > 400 ng/ml.
- Hình ảnh điển hình trên chụp CLVT ổ bụng có cản quang hoặc CHT có cản từ + AFP tăng cao hơn bình thường (chưa đến 400ng/ml) + nhiễm HBV hoặc HCV.
* Tiêu chuẩn lựa chọn điều trị can thiệp TACE và DEB-TACE (theo hướng dẫn điều trị UTBMTBG phân loại Barcelona giai đoạn B):
- Tổn thương còn chỉ định phẫu thuật cắt gan, ghép gan hoặc các biện pháp tiêu hủy khối u qua da nhưng bệnh nhân từ chối.
- Chức năng gan còn bù tốt (Child Pugh A, B), không có huyết khối tĩnh mạch cửa, không có shunt động tĩnh mạch gan và đồng ý tham gia nghiên cứu.
2.1.2. Tiêu chuẩn loại trừ:
- Xơ gan Child-Pugh C, ECOG 3-4 điểm. Có di căn ngoài gan, có huyết khối tĩnh mạch cửa. Đang chảy máu do vỡ giãn tĩnh mạch thực quản. Có rối loạn đông máu: tỉ lệ Prothrombin < 60%; Tiểu cầu < 50 G/l. Có bệnh nặng kết hợp (suy tim, suy thận, suy hô hấp) hoặc bệnh nhân quá già yếu. Phụ nữ có thai hoặc cho con bú. Các bệnh nhân bỏ theo dõi.
2.2. Phương pháp nghiên cứu: tiến cứu, can thiệp có đối chứng không ngẫu nhiên.
* Kỹ thuật can thiệp: Giống như các kỹ thuật can thiệp mạch truyền thống.
+ TACE: Lipiodol tính bằng ml, liều lipiodol bằng đường kính lớn nhất của khối u. Hoá chất chống ung thư Doxorubicin tính bằng ml (1 ml chứa 2 mg Doxorubicin) gấp 1,5 lần kích thước u tính bằng cm (1,5 ml Doxorubicin cho 1 cm đường kính khối u). Tạo nhũ tương Doxorubicin - lipiodol dưới áp lực của hai bơm tiêm 20ml và 10 ml, nối thông bằng một trạc ba. Bơm tắc động mạch nuôi khối u bằng Spongel: Spongel đã trộn nhuyễn với thuốc cản quang tan trong nước được bơm qua ống thông bằng bơm tiêm 1 ml cho đến khi nó dừng lại ở đầu ống thông. Tránh để Spongel bị trào ngược vào nhánh động mạch nuôi gan lành.
+ DEB-TACE: Các bước cơ bản tương tự như đối với hóa tắc mạch truyền thống. Hóa chất là Doxorubicin (Ebewe, Áo) được tải với hạt DC- Beads (Biocompatibles, Anh) 90-120 phút trước can thiệp. Liều hóa chất: Doxorubicin 50-150mg/lần can thiệp theo theo khuyến cáo chung, sử dụng 1 hoặc 2 trong 3 loại kích cỡ hạt DC-Beads (100-300µm, 300-500µm, 500-700µm).
* Chỉ tiêu nghiên cứu: Các chỉ số lâm sàng, AFP huyết thanh, đặc điểm khối u trên chẩn đoán hình ảnh, mức độ xơ gan theo Child Pugh, giai đoạn bệnh theo Okuda, Barcelona. Tính tỉ lệ sống thêm tích lũy tại các thời điểm 1 năm, 2 năm và 3 năm theo phương pháp Kaplan –Meier. Test log-rank được sử dụng để sử dụng để đánh giá sự khác biệt về thời gian và tỉ lệ sống thêm của các phân nhóm theo yếu tố tiên lượng.
* Xử lý số liệu: Sử dụng phần mềm SPSS 20.0.
III. KẾT QUẢ NGHIÊN CỨU
280 BN được thực hiện tổng cộng 648 lần hóa tắc mạch (121 bệnh nhân điều trị TACE với 346 lần can thiệp, trung bình 2,9 lần/1 bệnh nhân, nhiều nhất 10 lần và 159 bệnh nhân điều trị DEB-TACE với 305 lần can thiệp, trung bình 1,9 lần/1 bệnh nhân, nhiều nhất 5 lần), tất cả đều thành công về kỹ thuật. Thời gian theo dõi trung bình là 14,3 tháng (ngắn nhất 1,5 tháng, dài nhất 42 tháng).
3.1. Đặc điểm chung của nhóm nghiên cứu.
Bảng 3.1. Một số đặc điểm lâm sàng và cận lâm sàng của nhóm BN nghiên cứu.
|
Đặc điểm |
TACE (n=121) |
DEB-TACE (n= 159) |
p |
||||
|
Số lượng |
Tỉ lệ % |
Số lượng |
Tỉ lệ % |
||||
|
Tuổi trung bình |
59,37 ± 12,22 |
60,52 ± 12,65 |
0,6 |
||||
|
Nam/nữ |
115/6 |
148/11 |
0,34 |
||||
|
Yếu tố nguy cơ |
Không |
13 |
10,7 |
17 |
10,7 |
0,07 |
|
|
Virus B |
83 |
68,6 |
115 |
72,3 |
|||
|
Virus C |
5 |
4,1 |
14 |
8,8 |
|||
|
rượu |
9 |
7,4 |
2 |
1,3 |
|||
|
rượu + Virus B |
9 |
7,4 |
7 |
4,4 |
|||
|
Virus B + C |
2 |
1,7 |
4 |
2,5 |
|||
|
Triệu chứng lâm sàng |
Đau HSP |
90 |
74,4 |
131 |
82,4 |
0,14 |
|
|
Mệt mỏi |
65 |
53,7 |
69 |
43,4 |
0,09 |
||
|
RLTH |
27 |
22,3 |
26 |
16,4 |
0,21 |
||
|
Sút cân |
28 |
23,1 |
48 |
30,2 |
0,20 |
||
|
Gan to |
65 |
53,7 |
66 |
41,5 |
0,53 |
||
|
AFP huyết thanh |
Bình thường (≤ 20 ng/ml) |
40 |
33,0 |
59 |
37,2 |
0,48 |
|
|
Tăng (20-200ng/ml) |
29 |
24,0 |
43 |
27,0 |
|||
|
Tăng cao (>200ng/ml) |
52 |
43,0 |
57 |
35,8 |
|||
|
Độ biệt hóa |
Không sinh thiết |
81 |
66,9 |
9 |
5,7 |
0,09 |
|
|
Kém |
3 |
2,5 |
16 |
10,1 |
|||
|
Vừa |
16 |
13,2 |
58 |
36,5 |
|||
|
Cao |
7 |
5,8 |
33 |
20,8 |
|||
|
UTBMTBG khác |
14 |
11,6 |
43 |
27,0 |
|||
|
Số u gan |
1 khối |
105 |
86,8 |
97 |
61,0 |
0,045 |
|
|
2 khối |
6 |
5,0 |
30 |
18,9 |
|||
|
≥ 3 khối |
10 |
8,3 |
32 |
20,1 |
|||
|
Hình thái u |
Thể khối |
105 |
86,8 |
146 |
91,8 |
0,03 |
|
|
Thể nốt/đa ổ khu trú |
3 |
2,5 |
10 |
6,3 |
|||
|
Lan tỏa |
13 |
10,7 |
3 |
1,9 |
|||
|
Kích thước khối u |
< 8 cm |
61 |
50,4 |
75 |
47,2 |
0,5 |
|
|
≥ 8 cm |
60 |
49,6 |
84 |
52,8 |
|||
|
Kích thước khối u trung bình (cm) |
9,04 ± 4,49 |
9,28 ± 4,20 |
0,25 |
||||
|
Xơ gan theo Child-Pugh |
A |
115 |
95,0 |
154 |
96,9 |
0,44 |
|
|
B |
6 |
5,0 |
5 |
3,1 |
|||
|
Giai đoạn bệnh theo Okuda |
I |
70 |
57,9 |
99 |
62,3 |
0,46 |
|
|
II |
51 |
42,1 |
60 |
37,7 |
|||
|
Giai đoạn bệnh BCLC B theo Kinki |
B1 |
39 |
32,2 |
28 |
17,6 |
0,017 |
|
|
B2 |
81 |
66,9 |
129 |
81,1 |
|||
|
B3 |
1 |
0,8 |
2 |
1,3 |
|||
Nhận xét: Phần lớn các đặc điểm lâm sàng và cận lâm sàng của hai nhóm UTBMTBG nhóm TACE và DEB-TACE tương đương với nhau
3.2. Kết quả sống thêm lâu dài sau điều trị.
Bảng 3.2. Thời gian sống trung bình và tỉ lệ sống thêm theo các phân nhóm.
|
Phân nhóm |
TACE (n=121) |
DEB-TACE (n=159) |
p đơn biến |
p đa biến |
||||||
|
n |
OS |
n |
OS |
|||||||
|
Tuổi |
≤ 60 |
65 |
15,4 ± 1,6 |
71 |
21,2 ± 1,9 |
0,029 |
0,011 |
0,55 |
||
|
> 60 |
56 |
18,3 ± 1,8 |
88 |
21,6 ± 1,6 |
0,159 |
|||||
|
Giới |
Nam |
115 |
16,4 ± 1,3 |
148 |
20,8 ± 1,3 |
0,015 |
0,012 |
0,097 |
||
|
Nữ |
6 |
22,0 ± 0,6 |
11 |
30,1 ± 4,5 |
0,044 |
|||||
|
yếu tố nguy cơ |
Không |
13 |
16,8 ± 3,5 |
17 |
31,3 ± 3,6 |
0,014 |
0,009 |
0,554 |
||
|
Có |
108 |
17,2 ± 1,4 |
142 |
20,7 ± 1,3 |
0,072 |
|||||
|
AFP huyết thanh (ng/ml) |
BT ≤ 20 |
40 |
24,2 ± 2,4 |
59 |
24,0 ± 2,2 |
0,9 |
0,008 |
0,001 |
||
|
Tăng >20 |
81 |
13,4 ± 1,3 |
100 |
20,1 ± 1,4 |
0,001 |
|||||
|
Độ biệt hóa tế bào |
Kém |
3 |
6,8 ± 2,2 |
16 |
22,8 ± 3,9 |
0,005 |
0,026 |
0,007 |
||
|
Cao + vừa |
23 |
19,9 ± 2,5 |
91 |
23,3 ± 1,7 |
0,602 |
|||||
|
Kích thước khối u (cm) |
< 8 |
63 |
21,0 ± 1,8 |
75 |
24,8 ± 1,7 |
0,114 |
0,001 |
0,325 |
||
|
≥ 8 |
75 |
12,3 ± 1,4 |
84 |
18,7 ± 1,8 |
0,004 |
|||||
|
Hình thái u gan |
Thể khối |
105 |
18,9 ± 1,4 |
146 |
21,6 ± 1,3 |
0,136 |
0,01 |
0,114 |
||
|
nốt + lan tỏa |
16 |
5,36 ± 0,9 |
13 |
19,1 ± 3,4 |
0,001 |
|||||
|
Số lượng khối u gan |
1 u |
105 |
17,6 ± 1,4 |
97 |
24,0 ± 1,7 |
0,003 |
0,001 |
0,847 |
||
|
đa u |
16 |
11,8 ± 1,7 |
62 |
18,2 ± 1,8 |
0,133 |
|||||
|
Child-Pugh |
A |
115 |
16,9 ± 1,3 |
154 |
21,9 ± 1,3 |
0,004 |
0,009 |
0,538 |
||
|
B |
6 |
20,1 ± 5,3 |
5 |
9,7 ± 2,5 |
0,175 |
|||||
|
Okuda |
I |
70 |
19,4 ± 1,6 |
99 |
24,9 ± 1,6 |
0,032 |
0,007 |
0,002 |
||
|
II |
51 |
12,9 ± 1,8 |
60 |
16,7 ± 1,8 |
0,093 |
|||||
|
Kinki |
B1 |
39 |
20,9 ± 2,3 |
28 |
28,9 ± 2,6 |
0,026 |
0,001 |
0,20 |
||
|
B2 + B3 |
82 |
14,7 ± 1,3 |
131 |
19,9 ± 1,0 |
0,009 |
|||||
|
Đáp ứng mRECIST |
CR+PR |
32 |
26,8 ± 2,3 |
64 |
28,3 ± 2,0 |
0,585 |
0,024 |
0,001 |
||
|
SD+PD |
89 |
13,0 ± 1,2 |
95 |
17,3 ± 1,4 |
0,023 |
|||||
|
Phân tích đa biến theo mô hình hồi qui Cox Regression, số bước loại trừ nhiễu: 4 bước |
||||||||||
Nhận xét:
Tỉ lệ sống thêm tích lũy tại các thời điểm 1, 2, 3 năm: Nhóm TACE là: 52,1%; 25,0%, 13,9% và nhóm DEB-TACE là 65,3%; 42,6%, 24,1%. Thời gian sống thêm trung bình TACE là 17,1 ± 1,3 tháng, nhóm DEB-TACE là 21,6 ± 1,3 tháng (χ2= 7,1, p= 0,008)
Thời gian sống thêm không tiến triển bệnh trung bình nhóm TACE là 12,7 ± 1,3 tháng, nhóm DEB-TACE là 17,7 ± 1,4 tháng (χ2= 11,11, p= 0,001).
3.3. Các thông số liên quan đến thời gian sống thêm ở bệnh nhân UTBMTBG
Chúng tôi đã sử dụng một số các yếu tố liên quan đến nguy cơ tử vong ở bệnh nhân UTBMTBG được điều trị TACE và DEB-TACE. Biểu đồ 3.1 trình bày về các thông tin này.
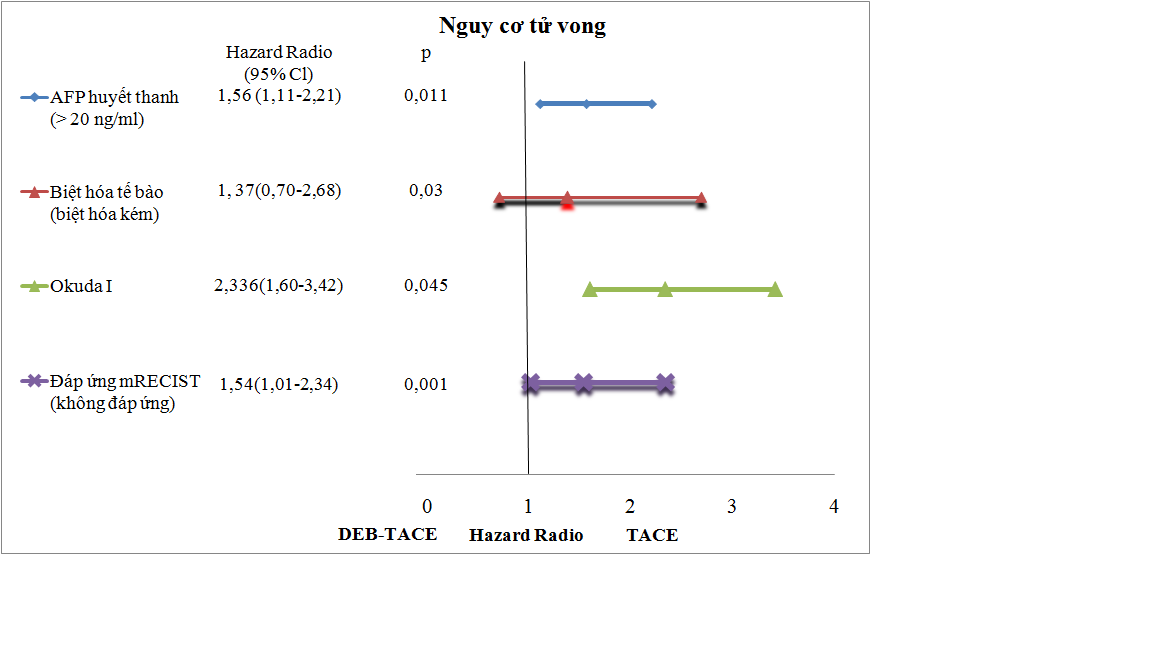
Biểu đồ 3.1. Tỉ số nguy cơ tử vong của các yếu tiên lượng.
Nhận xét: Độ biệt hóa tế bào, nồng độ AFP huyết thanh, giai đoạn bệnh Okuda I, đáp ứng sớm u gan (theo mRECIST) là các yếu tố dự báo tích cực đến kết quả sống thêm lâu dài của hai phương pháp điều trị.
IV. BÀN LUẬN.
4.1. Bàn về thời gian sống thêm của 2 nhóm điều trị: TACE và DEB-TACE
Hóa tắc mạch qua đường động mạch gan đã được chứng minh trong các thử nghiệm lâm sàng ngẫu nhiên có đối chứng là kéo dài được thời gian sống thêm cho bệnh nhân UTBMTBG không còn chỉ định phẫu thuật [4].
Tắc mạch vi cầu (DEB-TACE) với cơ chế tác dụng tiêu diệt khối u nổi trội hơn so với TACE. Hầu hết các kết quả nghiên cứu đều cho thấy hóa tắc mạch vi cầu cho tỉ lệ đáp ứng khối u tốt hơn, trong . Phân tích tổng hợp của Huang K (2014) trên 7 nghiên cứu với 700 BN cho thấy hóa tắc mạch vi cầu cho đáp ứng khối u tốt hơn (OR=1,92, CI95%[1,3-2,77], p=0,0004), tỉ lệ sống thêm 1 năm, 2 năm, 3 năm cũng cao hơn có ý nghĩa (p= 0,007,p = 0,0003 và p= 0,01) [6]. Lê Văn Trường thực hiện bằng kỹ thuật TACE cho 108 bệnh nhân UTBMTBG cho biết: thời gian sống thêm trung bình là 13 tháng, tỉ lệ sống thêm tại các thời điểm 1 năm, 2 năm và 3 năm lần lượt là 55,6%; 21,3% và 11,2% [4], kết quả nghiên cứu của Thái Doãn Kỳ trên 105 bệnh nhân UTBMTBG được điều trị DCB-TACE, thấy kết quả sống thêm trung bình của các bệnh nhân đạt 28 tháng, tỉ lệ sống thêm tại các thời điểm 1 năm, 2 năm và 3 năm lần lượt là 72,9%; 54,4% và 41,3% [7].
Trong nghiên cứu của chúng tôi, tỷ lệ sống thêm tích lũy tại các thời điểm 1 năm, 2 năm và 3 năm lần lượt nhóm TACE là: 52,1%; 25,0%, 13,9% và nhóm DEB-TACE là 65,3%; 42,6%, 24,1%. Thời gian sống thêm trung bình của nhóm TACE là 17,1 ± 1,3 tháng, nhóm DEB-TACE là 21,6 ± 1,3 tháng, sự khác nhau có ý nghĩa (χ2= 7,1, p= 0,008). Thời gian sống thêm không tiến triển bệnh trung bình của nhóm TACE là 12,7 ± 1,3 tháng, nhóm DEB-TACE là 17,7 ± 1,4 tháng, sự khác nhau có ý nghĩa (χ2= 11,11, p= 0,001). Những kết quả này đã cho thấy kỹ thuật DEB-TACE có hiệu quả cao hơn so với kỹ thuật TÊC đơn thuần, đặc biệt về thời gian sống của bệnh nhân sau điều trị.
4.1. Bàn về các yếu tố có liên quan đến thời gian sống 2 nhóm điều trị: TACE và DEB-TACE
Đánh giá các yếu tố tiên lượng về sống thêm lâu dài của UTBMTBG được điều trị TACE và DEB-TACE đã được đề cập trong nhiều báo cáo trong và ngoài nước. Các yếu tố tham gia đánh giá tiên luwownhgj sống bao gồm như: Giai đoạn bệnh theo Okuda, phân loại giai đoạn theo Barcelona; mức độ xơ gan theo Child Pugh, hàm lượng albumin, bilirubin, αFP huyết thanh và một số đặc điểm u gan (kích thước u, thể khối hay lan tỏa, xâm lấn mạch...) [7], [8], [9], [10], [11], [12]
Nghiên cứu của Lê Văn Trường cho biết có bảy yếu tố tiên lượng xấu đến thời gian sống của bệnh nhân UTBMTBG bao gồm: kích thước u > 10 cm, tuổi < 60, hàm lượng Albumin huyết thanh < 35 g/l, nồng độ Alpha-fetoprotein (AFP) huyết thanh, hình thái u lan tỏa, xâm lấn tĩnh mạch cửa, biệt hóa tế bào thấp – vừa… [4].
Thời gian sống thêm của bệnh nhân UTBMTBG phụ thuộc nhiều vào mức độ xơ gan theo phân loại Child-Pugh. Thời gian sống trung bình nhóm điều trị DEB-TACE giai đoạn Child-Pugh B trong nghiên cứu của chúng tôi là: 9,7 tháng.
Dựa trên phân tích đa biến đa biến theo mô hình hồi quy Cox Regression cho biết: Nguy cơ tử vong ở nhóm điều trị TACE tăng hơn so nhóm điều trị DEB-TACE liên quan đến nồng độ AFP huyết tăng (gấp 1,56 lần); độ biệt hóa tế bào nhóm biệt hóa kém (gấp 1,37 lần), phân loại giai đoạn bệnh Okuda I (gấp 2,34 lần), đáp ứng khối u sau lần điều trị đầu tiên theo phân loại mRECIST (gấp 1,54 lần), sự khác biệt có ý nghĩa với p <0,05.
Nghiên cứu Facciousso (2016) đánh giá yếu tố tiên lượng trên 104 bệnh nhân điều trị bằng TACE và 145 bệnh nhân điều trị bằng DEB-TACE phân nhóm Barcenola A và B cho biết các yếu tố như: Nồng độ AFP huyết thanh, bệnh nhân có 2 khối u gan, huyết khối tĩnh mạch cửa tăng cao có ý nghĩa ở nhóm điều trị TACE, với mức độ tăng lần luwoqwtj là: 2,29 lần, 2,5 lần và 1,75 lần [12]. Theo nghiên cứu của Song yếu tố nguy cơ độc lập có ý nghĩa là AFP < 200 ng/ml có giá trị tiên lượng với nguy cơ tử vong nhóm điều trị TACE cao gấp 1,72 lần so với DEB-TACE [14].
TÀI LIỆU THAM KHẢO
1. Bộ môn Ung thư - Trường Đại học Y Hà Nội (1997), Ung thư gan nguyên phát, Bài giảng ung thư học, Nhà xuất bản Y học, tr. 205.
2. Hiệp hội quốc tế chống ung thư (1991), "Ung thư học lâm sàng", Nhà xuất bản Y học, tr. 382-386.
3. Ulmer SC (2000), "Hepatocellular carcinoma: A concise guide to its status and mamagement", Postgrad Med, 107(5), pp. 117-124.
4. Lê Văn Trường (2006), "Nghiên cứu điều trị ung thư biểu mô tế bào gan kích thước trên 5 cm bằng phương pháp tắc mạch hóa dầu chọn lọc", Luận án Tiến sỹ Y học, Học viện Quân y.
5. Golfieri R., Giampalma E., Renzulli M., et al. (2014), "Randomised controlled trial of doxorubicin-eluting beads vs conventional chemoembolisation for hepatocellular carcinoma", British Journal of Cancer, 111(2), pp. 255-264.
6. Huang K, Zhou Q., Wang R., et al. (2014), "Doxorubicin-eluting beads versus conventional transarterial chemoembolization for the treatment of hepatocellular carcinoma", Journal of Gastroenterology and Hepatology, 29, pp. 920-925.
7. Thái Doãn Kỳ (2015), "Nghiên cứu kết quả điều trị ung thư biểu mô tế bào gan bằng phương pháp tắc mạch hóa chất sử dụng hạt vi cầu DC Beads", Luận án Tiến sỹ Y học, Viện Nghiên cứu Khoa học Y dược Lâm sàng 108.
8. Dương Minh Thắng (2009), "Nghiên cứu điều trị ung thư biểu mô tế bào gan bằng phương pháp tắc mạch hóa dầu kết hợp với tiêm Ethanol qua da", Luận án Tiến sỹ Y học, Học viện Quân y, tr. 51 - 52.
9. Nguyễn Tiến Thịnh (2011), "Nghiên cứu hiệu quả điều trị ung thư biểu mô tế bào gan bằng phương pháp tắc mạch hóa dầu đơn thuần và tắc mạch hóa dầu kết hợp đốt nhiệt sóng cao tần", Luận án tiến sĩ Y học, Viện nghiên cứu khoa học y dược lâm sàng 108, Hà Nội.
10. Dhanasekaran R, Kooby DA, Staley CA, et al. (2010), "Comparison of conventional transarterial chemoembolization (TACE) and chemoembolization with doxorubicin drug eluting beads (DEB) for unresectable hepatocelluar carcinoma (HCC)", J Surg Oncol, 101, tr. 476-480.
11. Suman A. (2014), "Factors Affecting Outcomes in Patients with Hepatocellular Carcinoma Treated with Transarterial Chemoembolization", Universal Journal of Clinical Medicine, 2(2), tr. 43 - 48.
12. Facciorusso A., Mariani L., Sposito C., et al. (2016), "Drug-eluting beads versus conventional chemoembolization for the treatment of unresectable hepatocellular carcinoma", Journal of Gastroenterology and Hepatology, 31(3), pp. 645-653.
13. Malagari K., Pomoni M., Moschouris H., et al. (2012), "Chemoembolization With Doxorubicin-Eluting Beads for Unresectable Hepatocellular Carcinoma: Five-Year Survival Analysis", Cardiovasc Intervent Radiol, 35, pp. 1119-1128.
14. Song MJ., Chun HJ., Song DS., et al. (2012), "Comparative study between Doxorubicin-eluting beads and conventional transarterial chemoembolization for treatment of hepatocellular carcinoma", Journal of Hepatology, 57(6), pp. 1244-1250.
Địa chỉ liên hệ:
BS Phạm Trung Dũng
Bệnh viện Bộ Xây Dựng
Tel: 0946.120.482
Email: [email protected]

- Optimal Screening Protocol after Liver Transplantation for HCC
- TIẾN BỘ MỚI TRONG PHÒNG TRỊ UNG THƯ GAN Ở VIỆT NAM
- HƯỚNG DẪN CỦA APASL 2024: VỀ CHẨN ĐOÁN & ĐIỀU TRỊ SUY GAN CẤP TRÊN NỀN GAN MẠN
- Khuyến cáo về Chẩn đoán và điều trị Ung thư đường mật vùng rốn gan ở Việt Nam
- KHUYẾN CÁO VỀ CHUYỂN ĐỔI SỐ VÀ TRÍ TUỆ NHÂN TẠO (AI) TRONG BỆNH LÝ GAN MẬT TỤY Ở VIỆT NAM
- Chiến lược điều trị Viêm gan virus B hiện nay
- Cập nhật tình hình Viêm gan Virus trên toàn cầu và các chính sách, khuyến cáo mới của WHO
- Chung tay Phòng trị Viêm gan và Ung thư gan tại Việt Nam
- Ứng dụng tiến bộ mới các dấu ấn sinh học virus và sự phát triển thuốc điều trị viêm gan B
- Modern Radiation Therapy Techniques in the Management of Liver Cancer – Pros & Cons : Proton, SBRT, and Y-90 microspheres
- Cập nhật xu hướng ứng dụng chuyển đổi số trong quản lý bệnh lý gan mạn tính trên thế giới và tại việt nam
- Cập nhật quản lý bệnh nhân Viêm gan virus B mạn
- “Đừng bỏ lỡ mục tiêu” “Don’t miss the target” chủ đề của ngày viêm gan thế giới 2023
- The Measures against hepatitis in Japan & future direction of measures against hepatitis in Vietnam
- Mang dịch vụ chăm sóc viêm gan đến gần hơn với cộng đồng – chúng ta đang ở đâu?
- CẬP NHÂT ĐIỀU TRỊ VIÊM GAN THEO HƯỚNG DẪN APASL 2023
- New HCC Screening Biomarkers Dr.Caviglia
- Cập nhật tình hình viêm gan vi rút trên toàn cầu và Việt Nam Chiến lược của WHO và quốc gia
- Advancement in cholangiocarcinoma management
- Hepatitis and Cirrhosis - the Pathway to Hepatocellular Carcinoma
- Liver transplantation in national children hospital
- living donor liver transplantation in Vinmec hospital
- Utility of HBcrAg in the diagnosis and prognosis of Hepatitis B progression
- Tối ưu hóa quản lý viêm gan virus B mạn hiện nay
- Giải phẫu bệnh trong chẩn đoán phân biệt HCC với các tổn thương tế bào gan dạng nốt
Tin cùng loại

 VN
VN
 EN
EN